RET基因是一种重要的肿瘤驱动基因,RET融合和突变发生在肺癌、甲状腺癌以及其他多种肿瘤类型中,在RET靶向药出现之前,针对RET融合和突变常见治疗手段包括RET靶向治疗、免疫治疗和化疗。免疫治疗及化疗在这类人群中疗效不足,而RET靶向治疗中,多靶点激酶抑制剂治疗,在抑制RET靶点的同时,也抑制其他激酶,致使靶点不够集中的,影响疗效,副作用相对较大。
2020年5月,FDA批准了首个高选择性RET靶向药塞普替尼(selpercatinib,LOXO-292),用于治疗多种实体瘤,包括NSCLC和甲状腺癌。在国内,塞普替尼于2019年11月首次获批临床,于2021年11月申报上市,并被纳入优先审评,加速其获批进程,于2022年10月获批上市。全球第二款获批的高选择性RET靶向药为普拉替尼(pralsetinib,BLU-667),与2021年3月首次在中国获批,用于治疗RET基因融合阳性的NSCLC患者。
那么塞普替尼和普拉替尼两种RET靶向药在化学结构及药理方面、疗效和安全性方面,以及在后续研发布局方面有何差异?本文将深入探讨,详细阐述。
01化学结构相似,抑制活性却大有差异?
塞普替尼和普拉替尼对不同的RET的抑制活性不同。IC50是一种评估药物对特定酶的抑制效果的测量指标,表示药物需要达到的浓度才能抑制该酶活性的一半。体外研究显示,塞普替尼的IC50显著小于普拉替尼,表明塞普替尼的抑制RET激酶的活性越高[1](图1)。

图1. 塞普替尼针对RET融合突变的IC50显著小于普拉替尼,表明对RET激酶的抑制活性更高
在耐药性方面,RET靶向治疗显著改善了驱动基因阳性NSCLC的治疗格局,但是获得性耐药问题一直困扰着临床医生,已成为亟待解决的重点难点问题。塞普替尼与普拉替尼两者的化学结构相似,但与RET激酶结合时空间构象上存在差别,导致了两种化合物对同种RET L730V/I耐药突变效果是不同的。
已有研究者探索分析了两个高选择性RET靶向药塞普替尼和普拉替尼的耐药问题,2021年的NPJ Precision Oncology杂志发表了一项临床前研究,显示了塞普替尼和普拉替尼对L730V/I RET顶端突变的不同活性[2]。
这项研究发现L730V/I RET突变对普拉替尼耐药,但对塞普替尼治疗敏感。L730V/I RET突变位于溶剂前沿的顶部。蛋白质-药物复合物的晶体结构显示,L730V/I突变导致了与普拉替尼更强的空间冲突,同样在动物模型中,研究者也发现了普拉替尼不能抑制BaF3/KIF5B-RET(L730V/I)细胞来源的移植瘤的生长,但塞普替尼可有效抑制这些肿瘤的生长(图2)[2]。
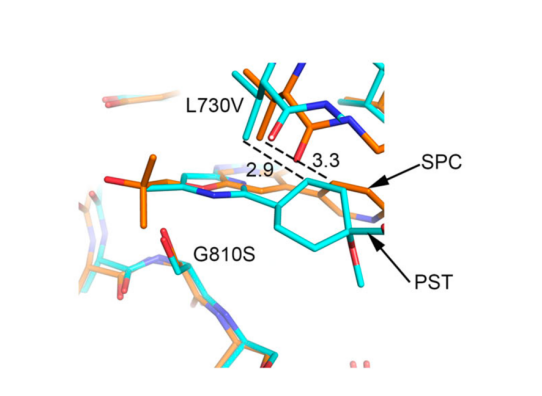
图2. 塞普替尼对RET L730V/I有抑制作用,而普拉替尼则无抑制作用
02 MAIC间接比较,两者到底孰优孰劣?
没有头对头的研究,如何比较塞普替尼和普拉替尼两款RET靶向药的疗效和安全性呢?
我们知道,罕见靶点研究领域较传统临床研究有诸多不同之处,主要体现在发病率低和检测技术不完善等方面,导致其很难像其他临床研究一样开展大型III期随机对照(RCT)的临床研究。因此,如何比较不同方案或不同药物在罕见靶点NSCLC患者中的疗效和安全性等问题是学术界亟需解决的问题。
2023年欧洲肺癌肿瘤大会上的一份研究报告通过匹配调整的间接比较(MAIC)方法,比较了针对塞普替尼的LIBRETTO-001研究(NCT03157128)[3]与针对普拉替尼的ARROW研究(NCT03037385)[4]两项研究的疗效和安全性[5]。两项研究均是针对于RET融合(+)晚期实体瘤患者的I/II期、单臂、开放标签全球研究,具有相似的入选和排除标准。在两项研究中,按照治疗阶段将NSCLC患者分为以下2组进行疗效分析:“初治”(TN)或“经铂类药物预治疗”(PP)。
结果显示,塞普替尼和普拉替尼对初治(TN)患者的疗效结局相似,但疗效和安全性都显示塞普替尼更有优势。具体来看:
疗效方面,加权后,治疗组之间的ORR相似。塞普替尼治疗组:中位PFS为22.1个月(95% CI,19.2-30.4),普拉替尼治疗组:中位PFS为13.3个月(95% CI,11.0-16.4),塞普替尼加权后的中位PFS更长,且在两个亚组中都观察到了这种趋势。在总体和TN人群中,塞普替尼和普拉替尼之间的OS没有显著差异。然而,在PP(经治)人群中,接受塞普替尼治疗的患者的OS有所延长(图3)。
安全性方面,接受塞普替尼的患者中≥3级TRAE发生率加权后为39.3%,而接受普拉替尼的患者≥3级TRAE发生率为62.6%(OR=0.39;95% CI,0.29-0.49);接受塞普替尼治疗的患者因TRAEs停止治疗加权后的发生率为3.6%,而接受普拉替尼的患者因TRAEs停止治疗的发生率为10%(OR=0.34;95% CI,0.14-0.58)(图3)。
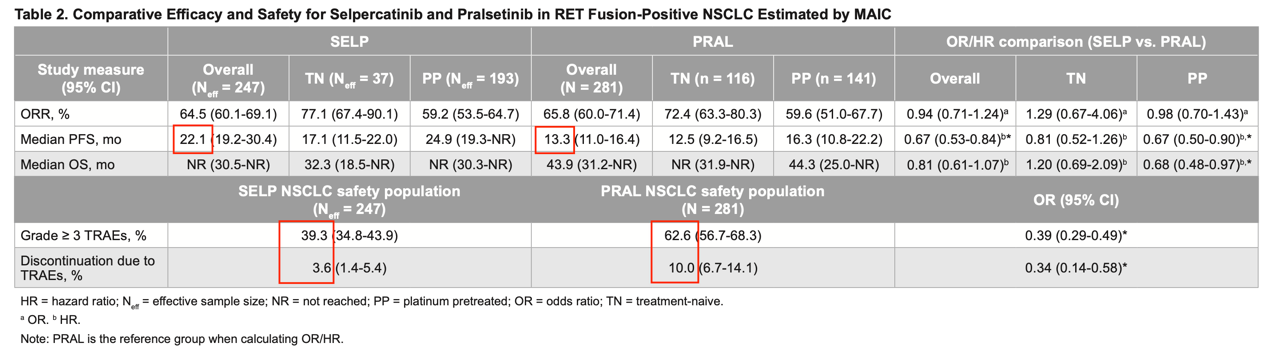
图3. MAIC评估的塞普替尼与普拉替尼治疗RET融合阳性NSCLC的疗效和安全性[5]
03塞普替尼一路高歌,普拉替尼却渐行渐远?
两款RET靶向药在化学结构和研究数据等方面已经有了孰优孰劣的客观数据提供,那么往远看,两款产品在整个研发布局方面是否有差距?
首先来看塞普替尼,2023ESMO上LIBRETTO-431(NCT04194944)和LIBRETTO-531(NCT04211337)两项III期研究成果公布,并同时发表在《新英格兰医学杂志》上[6,7]。RET靶向精准治疗迎来新突破。
LIBRETTO-431是一项针对未经治疗的RET融合阳性NSCLC患者的随机临床试验[6]。基于独立数据监查委员会(IDMC)所进行的预定中期疗效分析显示,该试验达成主要终点,在ITT–Pembrolizumab人群中,在预先计划的中期疗效分析时,塞普替尼组的中位PFS为24.8个月(95% CI,16.9-NE),对照组为11.2个月(95% CI,8.8-16.8)。进展/死亡风险降低54%(HR 0.46;P<0.001)。在基线时可测量的脑转移患者中,塞普替尼组颅内ORR为82%(95%CI,57-96),35%出现完全缓解(CR);对照组颅内ORR为58%(95%CI,28-85),CR率为17%。关于颅内反应中位持续时间的数据尚不成熟。LIBRETTO-531是首个比较高选择性RET激酶抑制剂塞普替尼与多激酶抑制剂卡博替尼/凡德他尼在RET突变的晚期或转移性甲状腺髓样癌(MTC)患者群体中的安全性和疗效的随机头对头试验[7]。经盲法独立中央审查(BIRC)的预定中期疗效分析,该研究达到了主要终点。BICR评估的中位PFS分别为NR vs 16.8个月,疾病进展或死亡风险显著降低72%(HR 0.28;P<0.001);塞普替尼组中位无治疗失败生存期暂未达到,对照组为13.9个月,因疾病进展、治疗相关不良事件导致的停用或死亡风险显著降低75%(HR 0.25;P<0.001)。
再来反观普拉替尼,在肺癌适应症中,NSCLC III期研究结果尚未公布,且该款RET靶向药并未进行针对早期NSCLC的探索;在MTC适应症的探索中也遭遇失败,在2023年6月29日,罗氏旗下的基因泰克宣布(该公司与Blueprint Medicines合作),主动撤回普拉替尼在美国的一项适应症:用于治疗12岁及以上晚期或转移性RET突变型MTC成人和儿童患者,2023年7月20日,美国FDA官网显示普拉替尼的该适应症已是撤回状态。
此外,塞普替尼还在早期NSCLC的辅助治疗领域进行了探索,塞普替尼的LIBRETTO-432研究首次将RET靶向药用于早期NSCLC患者的辅助治疗,如果这项研究能够顺利完成并达到主要终点,将为RET融合阳性NSCLC的早期患者带来更多治愈的希望。
因此,无论是从化学结构、已公布的研究数据,还是从整体适应症布局和研发进展的角度来看,塞普替尼和普拉替尼两者之间的差距已逐渐显现,从最初的不相上下,走向了渐行渐远。
参考文献:
1. Solomon BJ, et al. RET Solvent Front Mutations Mediate Acquired Resistance to Selective RET Inhibition in RET-Driven Malignancies. J Thorac Oncol. 2020;15(4):541-549.
2. Shen T, et al. The L730V/I RET roof mutations display different activities toward pralsetinib and selpercatinib. NPJ Precis Oncol. 2021;5(1):48.
3. Drilon A, et al. Selpercatinib in Patients With RET Fusion-Positive Non-Small-Cell Lung Cancer: Updated Safety and Efficacy From the Registrational LIBRETTO-001 Phase I/II Trial. J Clin Oncol. 2023;41(2):385-394.
4. Griesinger F, et al. Safety and efficacy of pralsetinib in RET fusion-positive non-small-cell lung cancer including as first-line therapy: update from the ARROW trial. Ann Oncol. 2022;33(11):1168-1178.
5. Maximilian H, et al. Matching-Adjusted Indirect Comparison (MAIC) of Treatment Outcomes for Selective RET Inhibitors, Selpercatinib, and Pralsetinib in Patients With Advanced Non-small Cell Lung Cancer (NSCLC). European Lung Cancer Congress 2023 27P.
6. Zhou C, et al. First-Line Selpercatinib or Chemotherapy and Pembrolizumab in RET Fusion-Positive NSCLC. N Engl J Med. 2023 Oct 21.
7. Hadoux J, et al. Phase 3 Trial of Selpercatinib in Advanced RET-Mutant Medullary Thyroid Cancer. N Engl J Med. 2023 Oct 21.







